Autorizan el uso de anticuerpos monoclonales como tratamiento para la COVID-19
Únete al canal de Whatsapp de Wapa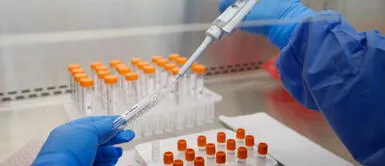
La Administración de Medicamentos y Alimentos (FDA) de Estados Unidos autorizó el uso de emergencia del bamlanivimab y etesevimab administrados juntos como tratamiento para el virus de la COVID-19.
El visto bueno es para pacientes confirmados con el coronavirus en estado leve a moderado que sean adultos o tengan más de 12 años de edad, con un peso mínimo de 40 kilogramos y que tienen un alto riesgo.
"El uso autorizado incluye el tratamiento para personas de 65 años o más o que padecen determinadas afecciones médicas crónicas", detalló la FDA en un comunicado.
En la investigación clínica se llevó a cabo una única perfusión intravenosa de bamlanivimab y etesevimab administrada simultáneamente, que redujo significativamente la hospitalización y la muerte relacionadas con el nuevo coronavirus.
Sin embargo, la entidad sanitaria de los Estados Unidos advirtió que aún siguen con la evaluación sobre la seguridad y eficacia de esta terapia en investigación para su uso en el tratamiento contra la COVID-19.
En esa misma línea, la FDA explicó que estos dos fármacos no están autorizados para pacientes contagiados con el virus que están hospitalizados, puesto que los enfermos con COVID-19 requieren oxigenoterapia y no se ha hecho un análisis sobre el mismo.
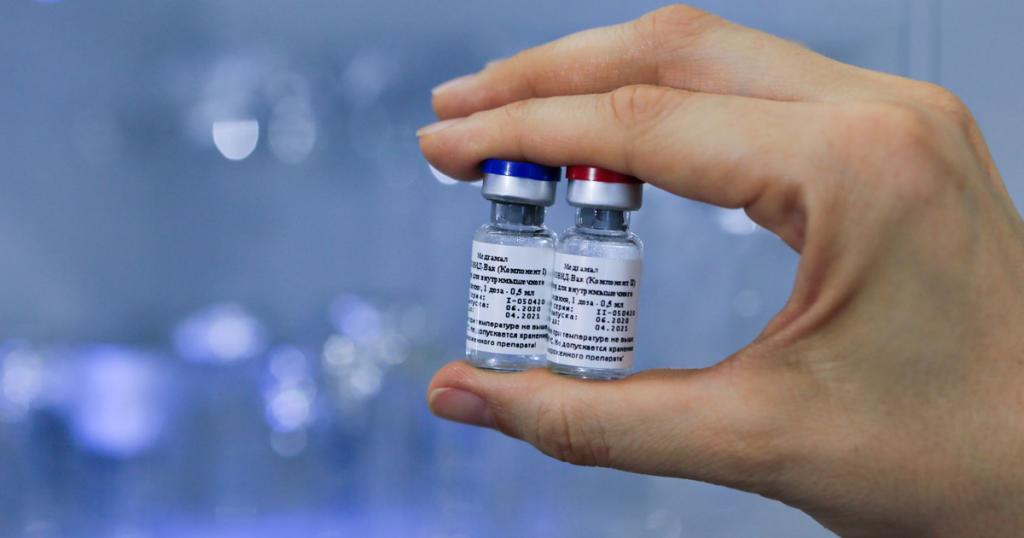
Asimismo, la entidad declaró que los anticuerpos monoclonales, como bamlanivimab y etesevimab, pueden estar asociados con peores resultados clínicos cuando se administran a pacientes que están en UCI.
"La acción, que proporciona otro tratamiento para la covid-19, refleja el fuerte compromiso de la FDA de trabajar con patrocinadores para expandir las posibles opciones de tratamiento que los proveedores de atención médica pueden usar para combatir esta pandemia", explicó Patrizia Cavazzoni, directora interina del Centro de la FDA para la Evaluación e Investigación de Medicamentos.
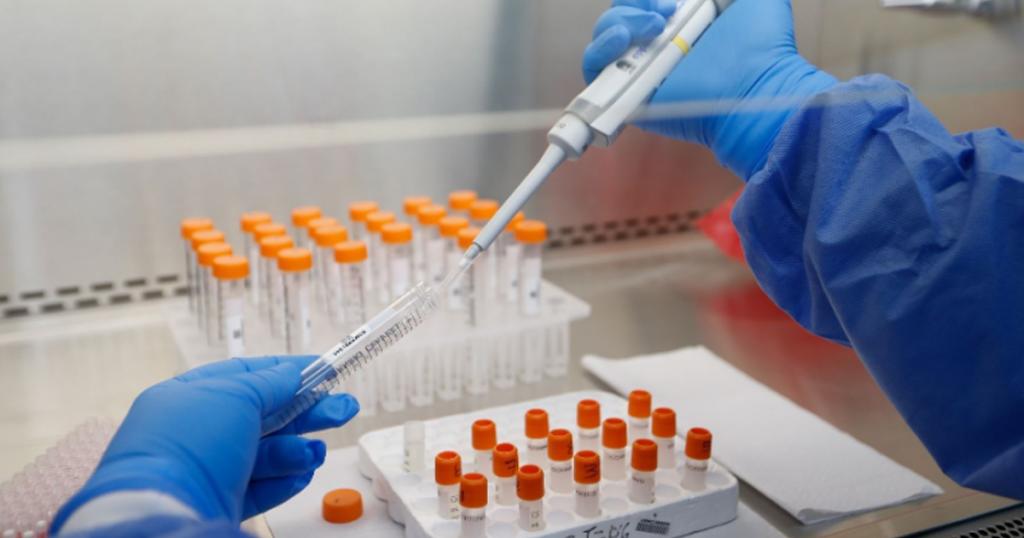
"Los datos que respaldan esta autorización de emergencia se suman a la evidencia emergente que apunta a la utilidad clínica de los anticuerpos neutralizantes para el tratamiento de la covid-19 en ciertos pacientes", acotó.
"Como parte de nuestro Programa de Aceleración del Tratamiento del Coronavirus, la FDA utiliza todos los recursos a nuestra disposición para hacer que tratamientos como estos anticuerpos monoclonales estén disponibles mientras continúa estudiando su seguridad y efectividad", precisó Cavazzoni.
De acuerdo con la entidad, estos anticuerpos monoclonales son proteínas elaboradas en laboratorio que imitan la capacidad del sistema inmunológico para combatir patógenos dañinos como los virus.










